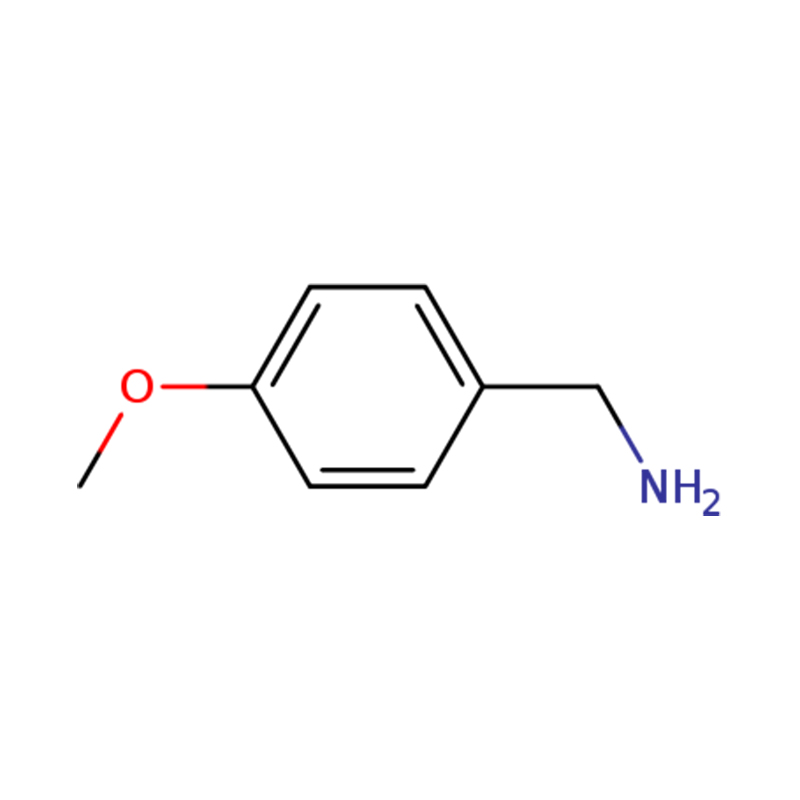
1-(4-METHOXYFENYL)METHANAMINE
Productdetails
| CasNo | 2393-23-9 | Levertijd | binnen 10 dagen |
| Moleculair | C8H11NO | Productiecapaciteit | 1 metrische ton/dag |
| Verschijning | Heldere, kleurloze tot lichtgele vloeistof | Zuiverheid | 99%min |
| Sollicitatie | Farmaceutische tussenproducten | Opslag | Kamertemperatuur, donker, afgesloten |
| LimietNum | 1 kilogram | Vervoer | Lucht, zee, expres. |
| Dikte | 1,05 g/mLat25°C(lit.) | Kookpunt | 236-237°C(lit.) |
| Smeltpunt | -10°C | Brekingsindex | n20/D1.546(lit.) |
| Vlampunt: | >110°C | Oplosbaarheid | Zeer goed oplosbaar in water |
| Naam | p-anisylamine of (4-methoxyfenyl)methanamine |
Synoniemen
LABOTEST-BB LTBB000703; AKOS BBS-00003589; 4-AMINOMETHYL-ANISOLE; 4-METHOXYBENZYLAMINE; P-Methoxybenzylaminehydrochloride 173,64; 4-Methoxybenzylamine, 98+%; voor Sparfloxacine; P-METHOXYBENZYLAMINEHYDROCHLORIDE
Sollicitatie
Het kan worden gebruikt voor de synthese van farmaceutische tussenproducten. Het is licht schadelijk voor water. Laat onverdunde of grote hoeveelheden producten niet in contact komen met grondwater, waterwegen of riolering. Lozing van materialen in het milieu zonder toestemming van de overheid is verboden om contact met oxiden, zuren, lucht en koolstofdioxide te voorkomen. Houd de verpakking gesloten, plaats deze in een luchtdichte afzuiger en bewaar op een koele, droge plaats.
QC-laboratorium
Op het terrein bevindt zich een apart QC-laboratorium waar chemische, fysische en microbiële tests, stabiliteitsonderzoeken en instrumenttests zoals IR, UV, HPLC en GC worden uitgevoerd op grondstoffen en eindproducten. De gehele ruimte is voorzien van toegangsbeveiliging en goed onderhouden, met voldoende analytische instrumenten voor de beoogde testdoeleinden. Alle instrumenten zijn goed geëtiketteerd en correct gekalibreerd.
QA
QA is verantwoordelijk voor het evalueren en categoriseren van de afwijking in Major, General en Minor. Voor alle niveaus van afwijkingen is onderzoek nodig om de grondoorzaak of potentiële oorzaak te identificeren. Het onderzoek moet binnen 7 werkdagen worden afgerond. De productimpactbeoordeling en het CAPA-plan zijn ook vereist nadat het onderzoek is afgerond en de grondoorzaak is vastgesteld. De afwijking wordt gesloten wanneer de CAPA is geïmplementeerd. Alle afwijkingen op niveau moeten worden goedgekeurd door de QA-manager. Na implementatie wordt de effectiviteit van de CAPA bevestigd op basis van het plan.